Артикул: 1043784
Раздел:Технические дисциплины (57837 шт.) >Химия (5274 шт.) >
Физическая химия (643 шт.)
Название или условие:
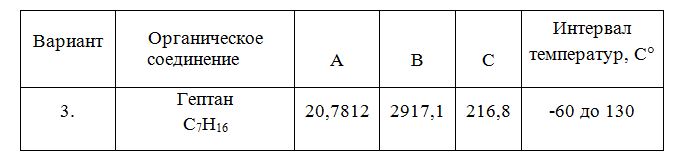
Используя зависимость давления насыщенного пара от температуры (см. таблицу 1), решите следующие задачи.
Задача 1. Вычислите нормальную температуру кипения жидкости (Тнтк).
Задача 2. Каким должно быть внешнее давление, чтобы жидкость закипела при 20°С?
Задача 3. Ненасыщенный пар охлаждается при постоянном давлении. При какой температуре начнется конденсация пара, если его давление равно 5,33·10 4 Па?
Задача 4. Вычислите теплоту испарения жидкости (по правилу Трутона) и расход энергии на перегонку одной тонны жидкости, допуская процесс идущим при нормальных условиях.
Задача 5. Вычислите среднюю теплоту испарения жидкости вблизи нормальной температуры кипения: от (Тнтк – 10) до Тнтк; сравните её с теплотой испарения, вычисленной по правилу Трутона. Сделайте вывод о справедливости правила Трутона.
Заданное вещество - Гептан
Описание:
Подробное решение в WORD
Изображение предварительного просмотра:
Процесс покупки очень прост и состоит всего из пары действий:
1. После нажатия кнопки «Купить» вы перейдете на сайт платежной системы, где можете выбрать наиболее удобный для вас способ оплаты (банковские карты, электронные деньги, с баланса мобильного телефона, через банкоматы, терминалы, в салонах сотовой связи и множество других способов)
2. После успешной оплаты нажмите ссылку «Вернуться в магазин» и вы снова окажетесь на странице описания задачи, где вместо зеленой кнопки «Купить» будет синяя кнопка «Скачать»
3. Если вы оплатили, но по каким-то причинам не смогли скачать заказ (например, случайно закрылось окно), то просто сообщите нам на почту или в чате артикул задачи, способ и время оплаты и мы отправим вам файл. Условия доставки: Получение файла осуществляется самостоятельно по ссылке, которая генерируется после оплаты. В случае технических сбоев или ошибок можно обратиться к администраторам в чате или на электронную почту и файл будет вам отправлен. Условия отказа от заказа: Отказаться возможно в случае несоответсвия полученного файла его описанию на странице заказа. Возврат денежных средств осуществляется администраторами сайта по заявке в чате или на электронной почте в течении суток.
