Артикул: 1036718
Раздел:Технические дисциплины (57837 шт.) >Химия (5274 шт.) >
Физическая химия (643 шт.)
Название или условие:
Возможно ли восстановление оксида висмута оксидом углерода при Т = 800 К по реакции (энтальпии образования (∆tH°) и энтропии (S°) веществ известны): Bi2O3 + 3CO = 2Bi + 3CO2; ∆tH°, кДж/моль -570,70, -110,53, 0, -393,51; S°, Дж(моль∙К) 151,49, 197,55, 56,9, 213,66
Описание:
Подробное решение
Изображение предварительного просмотра:
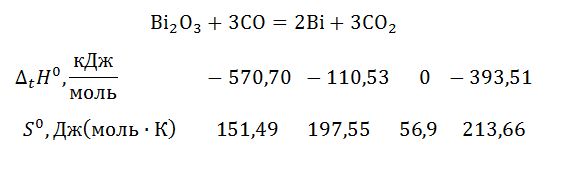
Процесс покупки очень прост и состоит всего из пары действий:
1. После нажатия кнопки «Купить» вы перейдете на сайт платежной системы, где можете выбрать наиболее удобный для вас способ оплаты (банковские карты, электронные деньги, с баланса мобильного телефона, через банкоматы, терминалы, в салонах сотовой связи и множество других способов)
2. После успешной оплаты нажмите ссылку «Вернуться в магазин» и вы снова окажетесь на странице описания задачи, где вместо зеленой кнопки «Купить» будет синяя кнопка «Скачать»
3. Если вы оплатили, но по каким-то причинам не смогли скачать заказ (например, случайно закрылось окно), то просто сообщите нам на почту или в чате артикул задачи, способ и время оплаты и мы отправим вам файл. Условия доставки: Получение файла осуществляется самостоятельно по ссылке, которая генерируется после оплаты. В случае технических сбоев или ошибок можно обратиться к администраторам в чате или на электронную почту и файл будет вам отправлен. Условия отказа от заказа: Отказаться возможно в случае несоответсвия полученного файла его описанию на странице заказа. Возврат денежных средств осуществляется администраторами сайта по заявке в чате или на электронной почте в течении суток.
